
实验证明,纯水有微弱的导电性。在298K时,纯水中H3O+的浓度为1.00×10-7 mol/L,说明水是弱电解质。水分子是一种两性物质,它既可给出质子,又可接受质子,于是在水分子间也可发生质子传递反应,称为水的质子自递反应。
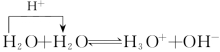
由于H3O+是强酸,OH-是强碱,H2O既是弱酸,又是弱碱,所以,水的质子自递反应进行得很微弱,建立平衡。其平衡常数式为:
![]()
在水的质子自递平衡中,因为反应很微弱,[H2O]可看成是常数,将它与K合并,于是
![]()
为了简便,通常用H+代表水合氢离子,即
![]()
Kw称为水的质子自递平衡常数,又称水的离子积。它表示在一定温度下的水溶液中H+浓度与OH-浓度的乘积是一个常数。
在298K时,纯水中H+和OH-浓度都是1.00×10-7 mol/L,所以
![]()
水的质子自递反应是一个吸热反应。Kw值随温度升高而增大,例如,0℃时为1.10×10-15;25℃时为1.00×10-14;100℃时为5.50×10-13。
水的离子积不仅适用于纯水,也适用于所有稀释溶液。因为水溶液中H+浓度和OH-浓度的乘积是一个常数,只要知道溶液中的H+浓度,就可以计算其中的OH-浓度。
如,0.10mol/L HCl溶液中,[H+]=0.10mol/L
而![]()
若0.010mol/L NaOH溶液中,[OH-]=0.010mol/L
则![]()





.jpg)
.jpg)
