
一、蛋白质等电点的测定
(一)实验目的
1.了解蛋白质的两性解离性质。
2.学习测定蛋白质等电点的一种方法。
(二)实验原理
蛋白质在酸性或碱性溶液中,分别带有正、负电荷,它们相互排斥,不容易发生沉淀。当溶液的pH值发生改变而使蛋白质分子所带正、负电荷数接近相等时,即失去同电相斥的作用。因此,蛋白质分子很容易彼此结合而沉淀,此时溶液的pH值称为该蛋白质的等电点。不同蛋白质各有其特异的等电点。在等电点时,蛋白质的理化性质都有变化,可利用此种性质的变化测定各种蛋白质的等电点。最常用的方法是测其溶解度最低时的溶液pH值。
本实验观察在不同pH值溶液中的溶解度以测定酪蛋白的等电点。用醋酸与醋酸钠(醋酸钠混合在酪蛋白溶液中)配制成各种不同pH值的缓冲液。向各缓冲溶液中加入酪蛋白后,沉淀出现最多的缓冲液的pH值即为酪蛋白的等电点。
(三)实验药品、实验设备
1.0.5%酪蛋白醋酸钠溶液50mL:称取纯酪蛋白0.25g置于50mL容量瓶内,准确加入蒸馏水20mL及1mol/L NaOH 5mL摇匀,使酪蛋白溶解,然后准确加入1mol/L醋酸溶液5mL,最后用蒸馏水稀释至刻度;
2.0.01mol/L醋酸;
3.0.1mol/L醋酸;
4.1 mol/L醋酸。
5.试管,试管架,移液管,50mL容量瓶。
(四)实验方法
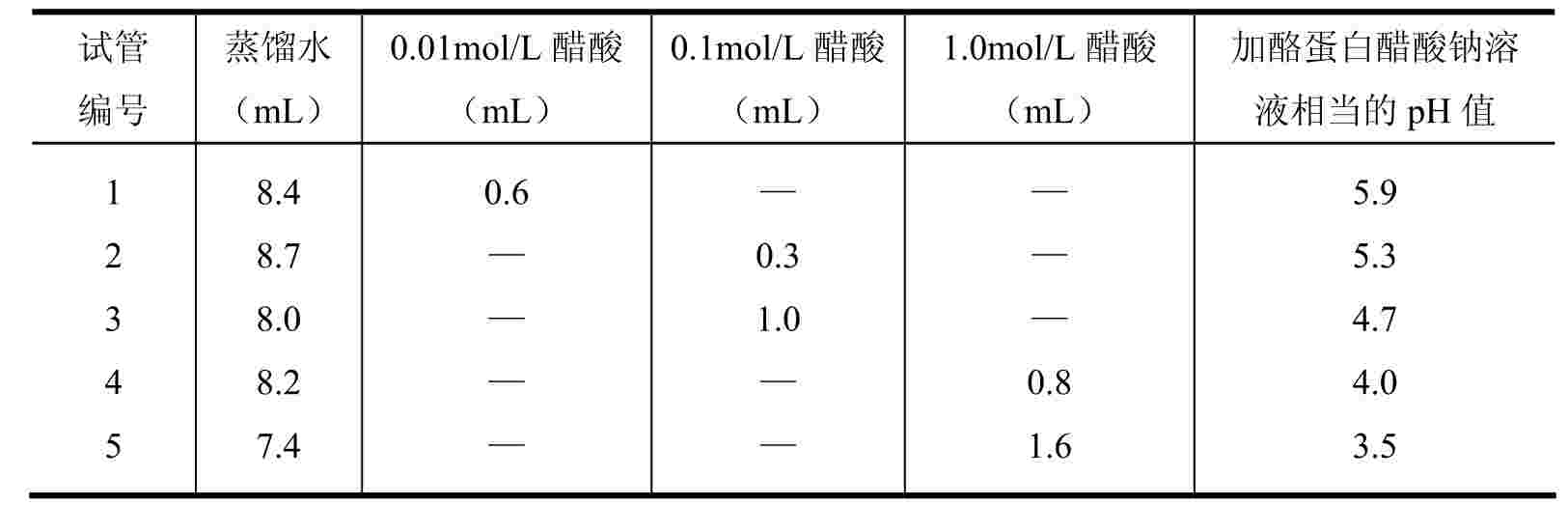
1.取同样规格的试管5支,按表2-5中要求,分别准确加入各试剂,混匀。表2-5中最末列为pH值参照数据。
2.加酪蛋白的醋酸钠溶液1mL,边加边摇动(切勿在各管加完后才摇动),pH值于各试管中依次为5.9、5.3、4.7、4.0、3.5,观察各管浑浊度,静置10~30min后,比较各管浑浊度。沉淀最多而且清液较透明的试管的pH值,即为酪蛋白的等电点。
表2-5 蛋白质等电点的测定
(五)实验记录
上一篇:腭部发育过程
下一篇:人体可以检测的皮质醇激素





.jpg)
.jpg)
